El 27 de setiembre de 2023, se publicó la Ley No. 31881 (en lo sucesivo, la Ley), que tiene por objeto brindar información de los alimentos que no contienen gluten en las etiquetas de los productos a fin de que los consumidores, principalmente, las personas que padecen de celiaquía, intolerancia o alegría al gluten, adopten decisiones de consumo informadas.
La Ley establece que las etiquetas de los productos que incluyan referencias como “libre de gluten” o “sin gluten” deberán cumplir con las condiciones que se establezcan en el respectivo Reglamento (aún no ha sido aprobado y el Ministerio de Salud tiene un plazo de 60 días calendario para aprobarlo) y los fabricantes deberán contar con un programa de buenas prácticas de fabricación establecido por DIGESA (tampoco ha sido aprobado). Asimismo, se indica que los fabricantes podrán consignar en los envases, recipientes, envoltorios o etiquetas de los productos que no contienen gluten, el símbolo de una espiga barrada dentro de un círculo, conforme a las características que se establezcan en el Reglamento de la Ley.
Asimismo, se establece que el incumplimiento de las disposiciones contenidas en la Ley dará lugar a una sanción, considerándose como agravante el hecho que el producto tenga características de alta difusión y consumo.
Finalmente, la Ley dispone un plazo de adecuación de 180 días calendario (el cual vencerá el 27 de marzo de 2024) a efectos que los proveedores, distribuidores o comerciantes, así como los productores o fabricantes, importadores o prestadores, y las empresas de alimentos se adecúan a lo dispuesto en la Ley.
Mediante la Resolución Ministerial No. 863-2023/MINSA, se aprobó la NTS N° 208-MINSA/DIGIESP-2023, “Norma Técnica de Salud que establece la vacunación contra la COVID-19”.
La Norma Técnica señala que el esquema de vacunación contra la Covid-19 que se administró en el territorio peruano con las vacunas monovalentes en el periodo 2021 hasta el mes de agosto de 2023 hace referencia al esquema inicial de vacunación para garantizar la respuesta inmunológica inicial suficiente.
De acuerdo con la evidencia científica y seguridad de la vacuna, el número de dosis es variable por año, dependiente del grupo priorizado y disponibilidad de la vacuna en el país.
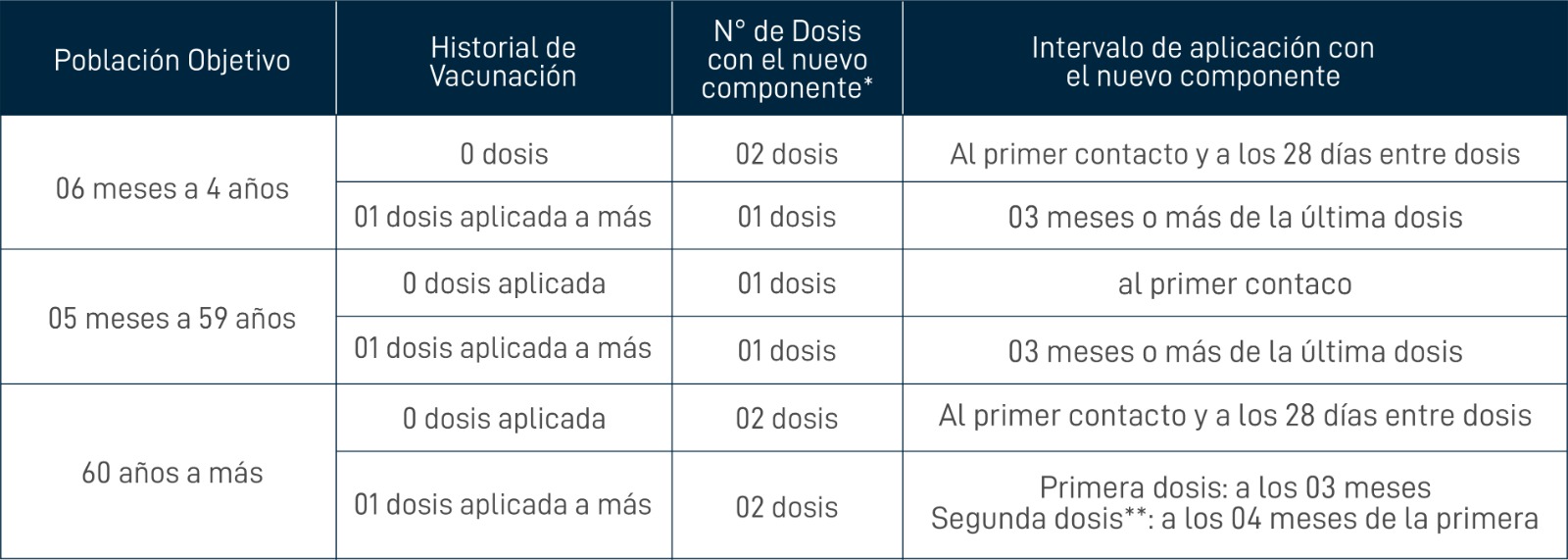
El nuevo esquema de vacunación es:
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) aprobó y autorizó el uso de nuevas vacunas contra el COVID-19 que protegen contra las nuevas variantes del virus.
Específicamente, las vacunas fabricadas por ModernaTX Inc. y Pfizer Inc. se han actualizado para incluir un componente monovalente que corresponde a la variante Omicron XBB.1.5.
Mediante la Ley No. 31870, se modificó la Ley No. 31336, Ley Nacional del Cáncer.
Las modificaciones más relevantes fueron: